基礎講座|pH中和処理制御技術 2-2. pHとは? 水素イオン濃度
ここで純粋な水に塩酸HClを加えて、水素イオン濃度が0.1(mol/L) の希塩酸を作ることを考えてみましょう。
水素原子1モルは1.0079gです。また、水素イオンというのは、水素原子から電子が1個はずれたものですから、
HCl → H+ + Cl-
H → H+ + e-
(水素原子) (水素イオン)(電子)
電子は、陽子の約1/1837の重さしかありません。計算上は水素イオンも水素原子も重さはほとんど変わらないので、水素原子量をそのまま使用してさしつかえありません。
したがって水素イオン1モルは、1.0079gとなります。水素イオン濃度0.1(mol/L)の希塩酸に含まれている水素イオンの量は、1.0079×0.1=0.10079(g/L)ということになります。
水素イオン濃度0.1(mol/L)溶液は、10-1(mol/L)でありその指数は-1です。
この指数の-を除いたものを水素イオン濃度指数{pH:ペーハー(独語)、ピーエイチ(英語)}といい、この場合1となります。
JIS規格では、ピーエイチ(英語)と定められていますが、一般的にはまだpH:ペーハー(独語)といわれています。
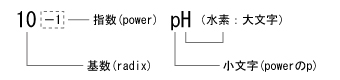
水素イオン濃度の指数(power)であるのでpowerの頭文字のp(小文字)をとり水素のHにつけてpHとされました。
この表示法によれば水素イオン濃度0.1(mol/L)の希塩酸のpHは1ということになります。純粋な水は、水素イオン濃度が10-7(mol/L)(at25℃)ですからpHは7ということになります。


