基礎講座|pH中和処理制御技術 4-2. ガラス電極 pH測定の原理・pH計の原理
pH測定の原理
前項(4-1. ガラス電極 ガラス電極を用いたpH測定)のように、薄いガラス膜を隔てて2種の溶液を接触させると、両液のpHの差に比例した電位差がガラス薄膜に発生します。両液のpHが同ーの時は、ガラス薄膜の両面における水素イオン濃度は同じであり、電位差は生じませんが、2つの溶液のpHが異なると、ガラス膜が2液と接している膜界面は水和した状態となり、電極内部液および被検液のそれぞれの水素イオン活量濃度と平衡し電位を発生します。
この結果、2つの間には電位差が発生します。
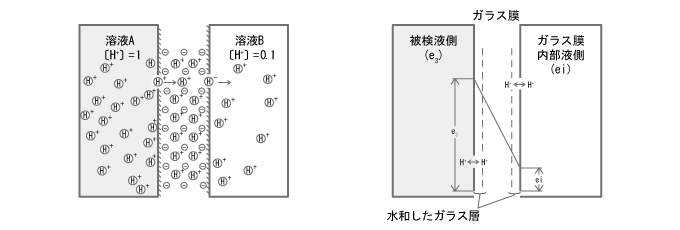
水素イオンの移動の模式図 ガラス膜模式図
pH計の原理
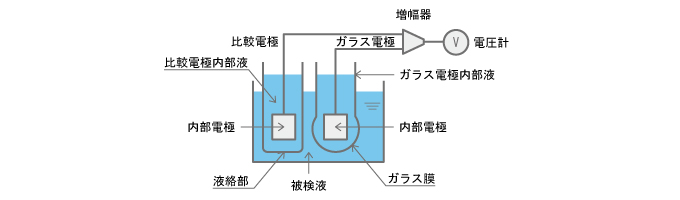
上記で、薄いガラス膜を隔てて2種の溶液を接触させると、両液のpHの差に比例した電位差がガラス薄膜の内側と外側に発生することをお話しました。
このガラス膜の内側(ガラス電極内部液)に発生する電位をガラス電極で測り、外側(被検液)に発生する電位を比較電極で測定します。
そして、このときの電位差をあらかじめpHの正確にわかったpH標準液で、測定したときの電位差と比較すれば、被検液のpHを知ることができるというわけです。
これがpH計の原理です。
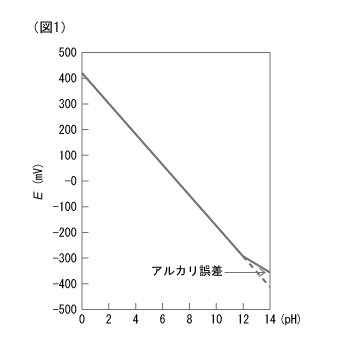
(図1)ガラス電極電位とpHとの関係
あらかじめpH値のわかった溶液(pH標準液)に電極を浸し、温度一定の条件の下でこの電位差(mV)とpHの関係を求めると(図1)のように膜電位差からpH値を知ることができます。
ここまでは、理論上の説明です。次回、実際にpH計を使用する際の注意点について説明していきます。


