基礎講座|滅菌・殺菌 12-4. 次亜塩素酸ナトリウムによる殺菌
上水道等における消毒法としては、処理規模・設備規模・操作性・安全性・コストなどのメリットにより、次亜塩素酸ナトリウム水溶液による殺菌が最も普及しています。
次亜塩素酸ナトリウムのメリット
- 殺菌効果が大きい。
- 取扱いが簡単で安定度が高く安全である。
- 殺菌効果の残留性が期待でき、残留塩素の測定が容易。
- 液体のため注入量の調整が容易で、自動制御による精度の高い管理が可能。
- 貯蔵設備(薬液タンク)の設置が簡単。
などが挙げられます。
次亜塩素酸ナトリウムの水中における作用
次亜塩素酸ナトリウムに殺菌力を持たせるためには、水溶液にする必要があります。
水溶液にすると、次亜塩素酸ナトリウム(NaClO)は水(H2O)と反応して、次亜塩素酸(HClO)と水酸化ナトリウム(NaOH)となります。
NaClO + H2O ⇔ HClO + NaOH ・・・(1)
塩素(Cl2)の場合は塩酸が生成しますが、次亜塩素酸ナトリウム水溶液の場合は水酸化ナトリウムが生成します。従って、液性はアルカリ側となり、pH値を上げる傾向になります。一方の次亜塩素酸(HClO)は不安定な化合物で、分解の際、強力な酸化作用を示す発生期の酸素を放出し、塩酸に変わります。
HClO + H2O ⇔ HCl + (O)・・・(2)
更に、この次亜塩素酸は水溶液中で、次亜塩素酸イオン(ClO-)と水素イオン(H+)とに解離します。
HClO ⇔ ClO- + H+ ・・・(3)
このイオン化の程度は水のpH値や水温によって変化します。
また、次亜塩素酸は水中にアンモニアやアンモニア誘導体などが存在するとそれらと反応して、クロラミン(クロルアミン)として知られている化合物をつくります。
このクロラミンは水中のpH値によって、モノクロラミン(NH2Cl)、ジクロラミン(NHCl2)、トリクロラミン(NCl3)に変化します。
残留塩素とは?
残留塩素とは、水中に残存する殺菌力を持った遊離塩素および結合塩素(クロラミン)をいいます。まとめると次のようになります。
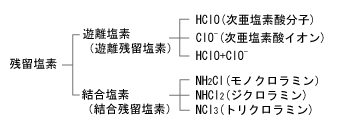
結合塩素は遊離塩素に比べて1桁ほど殺菌効果が落ちますが、反面、残留効果が長持ちすることになります。
また、同じ遊離塩素の中でも次亜塩素酸(HClO)の方が次亜塩素酸イオン(ClO-)に比べ、はるかに殺菌能力が大きいとされています。
例えば、EPA(米国環境庁)の報告では、塩素として0.1mg/Lのときの殺菌時間は、水温2~6℃で次亜塩素酸(HClO)を1とすると、次亜塩素酸イオン(ClO-)で80倍、NH2Cl(モノクロラミン)で350倍もの時間を要したとのことです。
次亜塩素酸ナトリウムの殺菌作用
次亜塩素酸ナトリウムによる殺菌のメカニズムは、水溶液にしたときの残留塩素が細菌や微生物の呼吸系酵素を阻害し、細胞の同化作用を停止させることにあり、生きている細胞を酸化させることではないとされています。
次亜塩素酸ナトリウムの殺菌作用に影響を与える因子
-
- pH値
- これは特に重要です。pH値が低いほど、HClOの割合が大きくなり、殺菌力が増すことになります。ここでいうpH値とは、次亜塩素酸ナトリウム注入後の値であることに注意する必要があります。アルカリ性によるpH値の上昇に留意してください。
-
- 水中の塩素消費物質の量
- アンモニア性窒素、還元性物質、酸化されやすい有機化合物などの影響を強く受けます。特に、アンモニア性窒素が存在すると、通常その存在量の7.5~10倍の塩素がクロラミンとなって消費されます。
-
- 水温
- 水温が上昇すると反応速度が高まり、殺菌作用も進行しますが、同時に残留塩素も分解、消耗されます。


